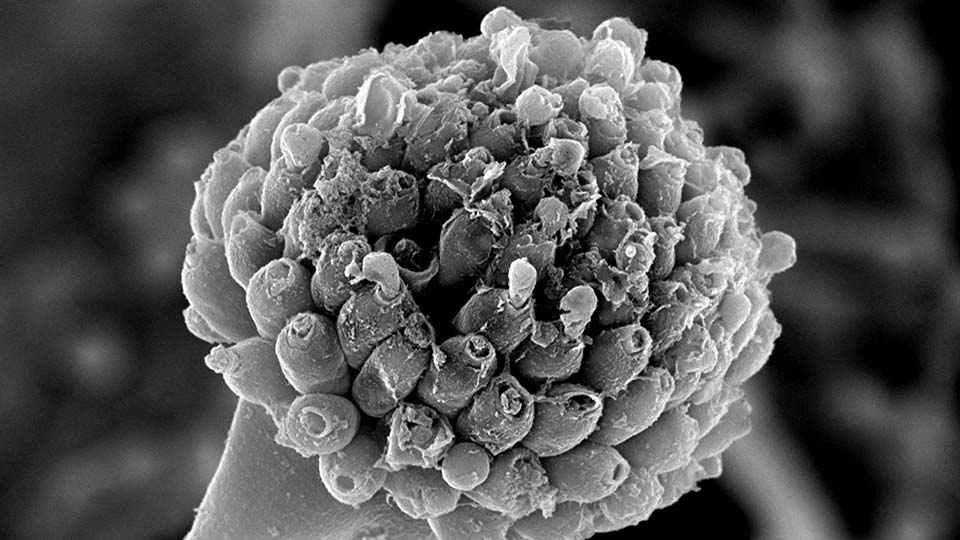
Ein neuartiger Mechanismus leitet den Zelltod ein
Pilzinfektionen sind insbesondere für Menschen mit einem geschwächten Immunsystem, zum Beispiel nach Transplantationen oder bei Chemotherapie eine große Gefahr, da Arzneimittel zur Behandlung von Pilzinfektionen häufig starke Nebenwirkungen haben oder Resistenzen auftreten können.
Zusammen mit Kolleginnen und Kollegen aus Japan haben Kieler Wissenschaftler unter Leitung von Prof. Jens-Michael Schröder Hautschuppen-Extrakte von Patientinnen und Patienten mit Psoriasis, einer Hautkrankheit mit überraschend seltenen Pilzinfektionen, analysiert. Dabei entdeckten sie, dass eine bestimmte Form des Proteins Psoriasin, das auf allen Körperoberflächen vorkommt, höchst wirksam gegen Pilze ist. „Überaschenderweise zeigt dieses körpereigene Fungizid einen völlig neuartigen Wirkmechanismus“, sagt Schröder.
Anders als bislang bekannte und gegen Pilze eingesetzte Therapeutika greift diese Form des körpereigenen Fungizids nicht direkt in den Stoffwechsel des Pilzes ein, sondern leitet über einen neuartigen, vom Spurenmetall Zink abhängigen Mechanismus den programmierten Zelltod (sogenannte Apoptose) in den Pilzzellen ein. Es dringt in die Pilzzellen ein und bindet als sogenannter Zink-Chelator im Zellinneren Zink. Dadurch werden in den Pilzzellen Mechanismen in Gang gesetzt, die den Zelltod einleiten. Im Tiermodell konnten die Autoren der Studie zeigen, dass sowohl das Psoriasin als auch ein entsprechender synthetisch hergestellter Zink-Chelator mit dem gleichen Wirkmechanismus Pilzinfektionen der Haut und der Lunge effektiv stoppen können.
Eine große Chance zur Bekämpfung von Pilzinfektionen
Die Ergebnisse dieser Studie seien eine große Chance zur Bekämpfung von oftmals tödlich verlaufenden Pilzinfektionen, sagt Schröder. „Der hier gefundene Wirkmechanismus bietet Ansatzmöglichkeiten für die Entwicklung neuer fungizider Therapeutika, die den programmierten Zelltod in Pilzzellen induzieren.“